溶液、溶質、溶劑是什么 溶液、溶質、溶劑的關系和區別
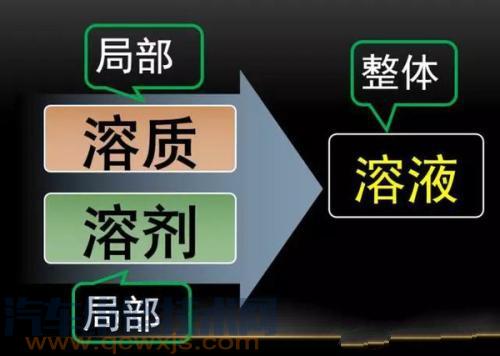
溶液
一種或一種以上的物質分散到另一種物質里,形成均一的、穩定的化合物,叫做溶液。
溶液除液態的外,還有氣態溶液和固態溶液。
溶劑
能溶解其他物質的物質叫做溶劑;
溶質
被溶解的物質叫做溶質。
在生活中常見的溶液有蔗糖溶液、碘酒、澄清石灰水、稀鹽酸、鹽水等。
水是常用的溶劑,水溶液是最重要的溶液。除水以外,其他的液體如酒精、汽油、苯、松節油等都是很好的有機溶劑,它們在涂料工藝中得到廣泛的應用。
溶液、溶質、溶劑的關系和區別
溶液中溶質、溶劑的區分方法
狀態區別
1、固+液固為質例:鹽水、碘酒
2、氣+液氣為質例:鹽酸中氯化氫為質
3、液+液量少為質例:工業酒精(少量甲醇溶于乙醇)
4、物+水水永為劑例:5%或95%酒精溶液
溶劑非水的溶液:(1)碘灑(2)空氣(3)合金
名稱區分
溶質的溶劑溶液例:碘的酒精溶液
2、溶質溶液(溶劑為水)例:硫酸銅溶液液配制
1、配制10g5%食鹽溶液(固配液)步驟:計算、稱量量取、攪拌溶解2、用37%的濃鹽酸配制50g5%稀鹽酸(液配液)步驟:計算、量取、混合飽和溶液和不飽和溶液之間的轉化關系
飽和溶液轉化為不飽和溶液的方法:1、加溶劑至溶質完全溶解2、升溫至溶質完全溶解
不飽和溶液轉化為飽和溶液方法:1、蒸發溶劑至溶質剛析出2、加溶質至不再溶解
3、降溫至剛有溶質析出
判斷溶液是否飽和的方法:1、完全溶解后看是否有不溶的固體溶質存在;
2、向溶液中加一定量溶質,看溶質質量是否減少
*濃溶液(稀溶液)不一定是飽和溶液(不飽和溶液);但同溫度下,同種溶質的飽和溶液一定比其不飽和溶液的濃度要濃
- 前文: 純凈物和混合物的定義及區別
- 后文: 汽車清洗步驟 汽車清洗流程